Mes paniers
Vous n'avez encore rien dans votre panier
Mes paniers
Vous n'avez encore rien dans votre panier

{{getOldPrice()}}{{getPrice()}}
 ¡ En achetant ce produit, vous devez {{calculatedProductMenttos()}} menttos !
¡ En achetant ce produit, vous devez {{calculatedProductMenttos()}} menttos !
Sans gluten

Végétalien

Sans gluten

Végétalien
L'infusion de boldo est très digestive et aide à réparer le foie et la vésicule biliaire
Il stimule la production de bile (il peut doubler le flux de bile) et l'écoulement du liquide de la vésicule biliaire, ce qui facilite la digestion et combat les symptômes résultant d'un dysfonctionnement du foie ou de la vésicule biliaire (flatulences et spasmes intestinaux).
L'infusion de boldo est très digestive et aide à réparer le foie et la vésicule biliaire
Boldo (POEMUS BOLDUS) feuilles entières/hachées
Boldo (POEMUS BOLDUS) feuilles entières/hachées
L'infusion de boldo est très digestive et répare le foie et la vésicule biliaire. Les feuilles de boldo peuvent être prises seules ou en association avec d'autres plantes digestives. Dissoudre une cuillère à soupe de boldo ou un mélange de plantes dans un demi-verre d'eau et laisser reposer toute la nuit. Le lendemain, ajoutez quelques gouttes de jus de citron. Avant de prendre la préparation, prenez une cuillère à café d'huile d'olive pour stimuler la vidange de la vésicule biliaire
La consommation de boldo stimule la production de bile (elle peut doubler le débit biliaire) et l'écoulement du liquide de la vésicule biliaire, ce qui favorise la digestion et combat les symptômes résultant d'un dysfonctionnement du foie ou de la vésicule biliaire (flatulences et spasmes intestinaux)
PROPERTIES:
/p>
Digestive, cholagogue (expulsion de la bile) et diurétique. A forte dose, il est anesthésiant et hypnotique
INDICATIONS:
Indications:
Indications :
Hépatite, insuffisance hépato-biliaire, lithiase biliaire, colique hépatique. Spasmes digestifs, dyspepsie hyposécrétoire. L'insomnie. Cystite
PRECAUTIONS:
Ne pas utiliser en traitement prolongé. Des doses élevées peuvent produire un effet narcotique.
Ne pas utiliser en traitement prolongé
CONTRAINDICATIONS: CONTRAINDICATIONS: Grossesse et grossesse
Grossesse et allaitement
(SOURCE : VADEMECUM PLANTAS MEDICINALES PLAMECA) (SOURCE : VADEMECUM PLANTAS MEDICINALES PLAMECA) Conservation
Conserver dans un endroit frais et sec, à l'abri des odeurs fortes et des sources de contamination
DECLARATION DES ALLERGES DECLARATION DES ALLERGES Selon la fiche technique
Selon la fiche technique du ou des fournisseurs :
Il ne contient AUCUN GLUTEN EN TANT QU'INGRÉDIENT, Mais AUCUNE GARANTIE NE PEUT ÊTRE DONNÉE SUR L'ABSENCE DE TRACE. ALLERGÈNES:
Ne contient aucun allergène comme ingrédients
En raison d'une contamination croisée, peut contenir Célériaque, noix, moutarde et sésame
Des processus de nettoyage et d'assainissement sont effectués tant dans nos installations que dans celles de nos fournisseurs après chaque production pour éviter toute contamination croisée, ainsi que des systèmes d'autocontrôle et de vérification pour confirmer l'absence de traces. Cependant, nous ne pouvons pas affirmer que les produits sont exempts d'allergènes présents dans la plante en raison d'une contamination accidentelle
DIRECTIVE COMMUNAUTAIRE 2006/142/CE RELATIVE AUX INGRÉDIENTS ET À L'ÉTIQUETAGE DES ALLERGÈNES
Selon la directive 2003/89/CE, voici la liste des ingrédients allergènes qui doivent être mentionnés sur l'étiquetage à des fins de protection des consommateurs, car la présence de ces substances peut provoquer des allergies. 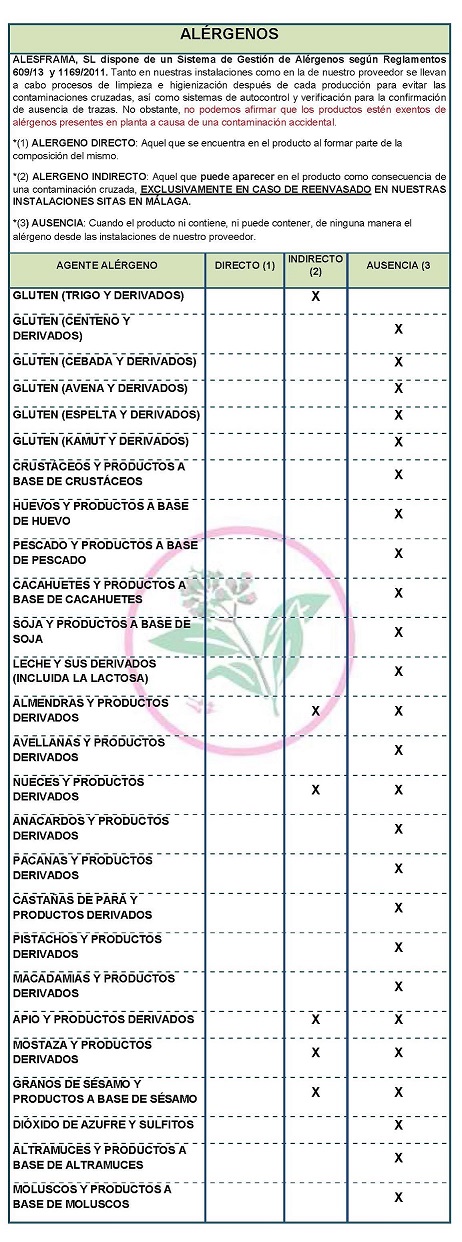
DECLARATION DE NON-MODIFICATION GÉNÉTIQUE
LÉGISLATION APPLICABLE
APTITUDE POUR LES GROUPES ETHNIQUES ET AUTRES:
HALAL convient : OUI, certificat officiel non disponible
Approuvé par les diététiciens : OUI
convient aux végétariens : Oui
Plaisant pour les végétariens : Oui
SUIT POUR LES CELIACS : NON
NON
SUIT POUR LES CELIACS : NON
L'infusion de boldo est très digestive et aide à réparer le foie et la vésicule biliaire
Il stimule la production de bile (il peut doubler le flux de bile) et l'écoulement du liquide de la vésicule biliaire, ce qui facilite la digestion et combat les symptômes résultant d'un dysfonctionnement du foie ou de la vésicule biliaire (flatulences et spasmes intestinaux).
L'infusion de boldo est très digestive et aide à réparer le foie et la vésicule biliaire
Boldo (POEMUS BOLDUS) feuilles entières/hachées
Boldo (POEMUS BOLDUS) feuilles entières/hachées
L'infusion de boldo est très digestive et répare le foie et la vésicule biliaire. Les feuilles de boldo peuvent être prises seules ou en association avec d'autres plantes digestives. Dissoudre une cuillère à soupe de boldo ou un mélange de plantes dans un demi-verre d'eau et laisser reposer toute la nuit. Le lendemain, ajoutez quelques gouttes de jus de citron. Avant de prendre la préparation, prenez une cuillère à café d'huile d'olive pour stimuler la vidange de la vésicule biliaire
La consommation de boldo stimule la production de bile (elle peut doubler le débit biliaire) et l'écoulement du liquide de la vésicule biliaire, ce qui favorise la digestion et combat les symptômes résultant d'un dysfonctionnement du foie ou de la vésicule biliaire (flatulences et spasmes intestinaux)
PROPERTIES:
/p>
Digestive, cholagogue (expulsion de la bile) et diurétique. A forte dose, il est anesthésiant et hypnotique
INDICATIONS:
Indications:
Indications :
Hépatite, insuffisance hépato-biliaire, lithiase biliaire, colique hépatique. Spasmes digestifs, dyspepsie hyposécrétoire. L'insomnie. Cystite
PRECAUTIONS:
Ne pas utiliser en traitement prolongé. Des doses élevées peuvent produire un effet narcotique.
Ne pas utiliser en traitement prolongé
CONTRAINDICATIONS: CONTRAINDICATIONS: Grossesse et grossesse
Grossesse et allaitement
(SOURCE : VADEMECUM PLANTAS MEDICINALES PLAMECA) (SOURCE : VADEMECUM PLANTAS MEDICINALES PLAMECA) Conservation
Conserver dans un endroit frais et sec, à l'abri des odeurs fortes et des sources de contamination
DECLARATION DES ALLERGES DECLARATION DES ALLERGES Selon la fiche technique
Selon la fiche technique du ou des fournisseurs :
Il ne contient AUCUN GLUTEN EN TANT QU'INGRÉDIENT, Mais AUCUNE GARANTIE NE PEUT ÊTRE DONNÉE SUR L'ABSENCE DE TRACE. ALLERGÈNES:
Ne contient aucun allergène comme ingrédients
En raison d'une contamination croisée, peut contenir Célériaque, noix, moutarde et sésame
Des processus de nettoyage et d'assainissement sont effectués tant dans nos installations que dans celles de nos fournisseurs après chaque production pour éviter toute contamination croisée, ainsi que des systèmes d'autocontrôle et de vérification pour confirmer l'absence de traces. Cependant, nous ne pouvons pas affirmer que les produits sont exempts d'allergènes présents dans la plante en raison d'une contamination accidentelle
DIRECTIVE COMMUNAUTAIRE 2006/142/CE RELATIVE AUX INGRÉDIENTS ET À L'ÉTIQUETAGE DES ALLERGÈNES
Selon la directive 2003/89/CE, voici la liste des ingrédients allergènes qui doivent être mentionnés sur l'étiquetage à des fins de protection des consommateurs, car la présence de ces substances peut provoquer des allergies. 
DECLARATION DE NON-MODIFICATION GÉNÉTIQUE
LÉGISLATION APPLICABLE
APTITUDE POUR LES GROUPES ETHNIQUES ET AUTRES:
HALAL convient : OUI, certificat officiel non disponible
Approuvé par les diététiciens : OUI
convient aux végétariens : Oui
Plaisant pour les végétariens : Oui
SUIT POUR LES CELIACS : NON
NON
SUIT POUR LES CELIACS : NON
