Mes paniers
Vous n'avez encore rien dans votre panier
Mes paniers
Vous n'avez encore rien dans votre panier

{{getOldPrice()}}{{getPrice()}}
 ¡ En achetant ce produit, vous devez {{calculatedProductMenttos()}} menttos !
¡ En achetant ce produit, vous devez {{calculatedProductMenttos()}} menttos !
Sans gluten

Végétalien

Sans gluten

Végétalien
Les feuilles de bouleau sont utilisées depuis l'Antiquité pour traiter les rhumatismes, la goutte et les maladies du système urinaire. Les tisanes sont préparées par décoction d'une ou deux cuillères à soupe de feuilles séchées par tasse d'eau, en ajoutant une pincée de bicarbonate de soude. L'infusion a une odeur aromatique et un goût amer.
La BOURGEOISE (BETULA ALBA L.) FEUILLES COUPÉES
La BEDULE (BETULA ALBA L.)
Les feuilles de bouleau sont utilisées depuis l'Antiquité pour le traitement des rhumatismes, de la goutte et des maladies du système urinaire. Les tisanes sont préparées par décoction d'une ou deux cuillères à soupe de feuilles séchées par tasse d'eau, en ajoutant une pincée de bicarbonate de soude. L'infusion a une odeur aromatique et un goût amer. Elles contiennent des saponines, des huiles essentielles, des tanins et des antiseptiques végétaux (phytosides)
Les feuilles de bouleau ont des propriétés diurétiques reconnues, utiles dans le traitement des affections rhumatismales et de la goutte (acide urique). Il produit une élimination rénale qui n'irrite pas les reins. (usage interne) Traitement des œdèmes d'origine cardio-rénale. (usage interne) Active la fonction rénale. (usage interne)
PROPERTIES:
Diurétique, anti-inflammatoire, fébrifuge, astringent
INDICATIONS:
Troubles urinaires, rhumatismes, œdèmes, fièvre, dyskinésies biliaires
PRECAUTIONS:
Non décrites
Non décrit.
Précautions
CONTRAINDICATIONS: Non décrit
Non décrit
(SOURCE : VADEMECUM PLANTAS MEDICINALES PLAMECA) (SOURCE : VADEMECUM PLANTAS MEDICINALES PLAMECA) L'infusion de feuilles de bouleau est un puissant diurétique capable de dissoudre les calculs rénaux et vésicaux, pour lesquels il est recommandé d'ajouter une pincée de bicarbonate de sodium à l'infusion. (SOURCE : VADEMECUM PLANTAS MEDICALES PLAMECA) Non décrit
Utilisations : Utilisation :
Les teasins sont préparés par décoction d'une ou deux cuillères à soupe de feuilles séchées par tasse d'eau, en ajoutant une pincée de bicarbonate de soude. L'infusion a une odeur aromatique et un goût amer. Elles contiennent des saponines, des huiles essentielles, des tanins et des antiseptiques végétaux (phytosides)
Conservation
Conserver dans un endroit frais et sec, à l'abri des odeurs fortes et des sources de contamination Stockage
Stockage Conserver dans un endroit frais et sec, à l'abri des odeurs fortes et des sources de contamination. DECLARATION DES ALLERGES DECLARATION DES ALLERGES
Selon la fiche technique du ou des fournisseurs :
Il ne contient AUCUN GLUTEN EN TANT QU'INGRÉDIENT, Mais AUCUNE GARANTIE NE PEUT ÊTRE DONNÉE SUR L'ABSENCE DE TRACE.
ALLERGÈNES:
Ne contient aucun allergène comme ingrédients
En raison d'une contamination croisée, peut contenir Célériaque, noix, moutarde et sésame
Des processus de nettoyage et d'assainissement sont effectués tant dans nos installations que dans celles de nos fournisseurs après chaque production pour éviter toute contamination croisée, ainsi que des systèmes d'autocontrôle et de vérification pour confirmer l'absence de traces. Cependant, nous ne pouvons pas affirmer que les produits sont exempts d'allergènes présents dans la plante en raison d'une contamination accidentelle
DIRECTIVE COMMUNAUTAIRE 2006/142/CE RELATIVE AUX INGRÉDIENTS ET À L'ÉTIQUETAGE DES ALLERGÈNES Selon la directive 2003/89/CE, voici la liste des ingrédients allergènes qui doivent être mentionnés sur l'étiquetage à des fins de protection des consommateurs, car la présence de ces substances peut provoquer des allergies. DECLARATION DE NON-MODIFICATION GÉNÉTIQUE LÉGISLATION APPLICABLE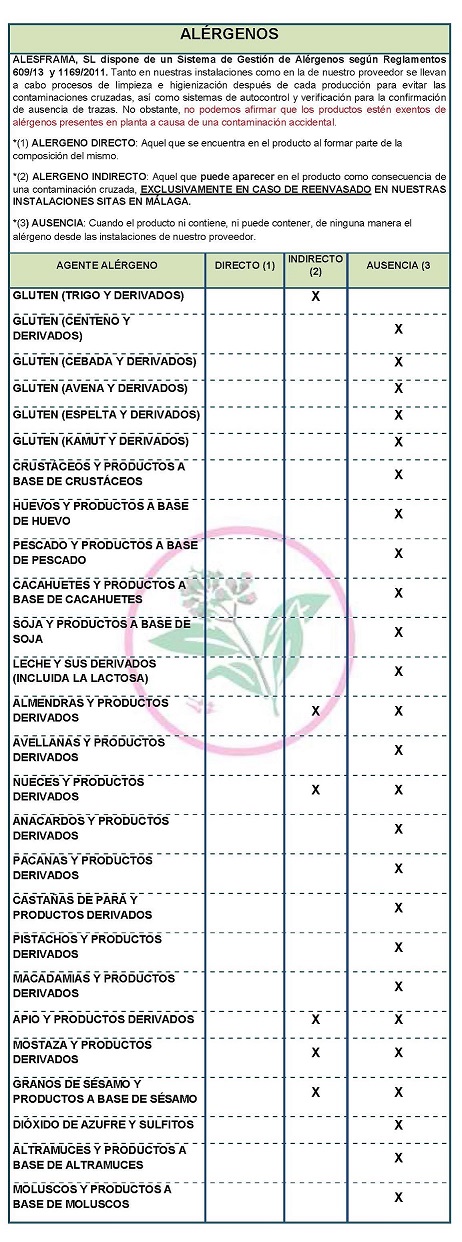
APTITUDE POUR LES GROUPES ETHNIQUES ET AUTRES:
HALAL convient : OUI, certificat officiel non disponible
Approuvé par les diététiciens : OUI
convient aux végétariens : Oui
Plaisant pour les végétariens : Oui
SUIT POUR LES CELIACS : NON
Les feuilles de bouleau sont utilisées depuis l'Antiquité pour traiter les rhumatismes, la goutte et les maladies du système urinaire. Les tisanes sont préparées par décoction d'une ou deux cuillères à soupe de feuilles séchées par tasse d'eau, en ajoutant une pincée de bicarbonate de soude. L'infusion a une odeur aromatique et un goût amer.
La BOURGEOISE (BETULA ALBA L.) FEUILLES COUPÉES
La BEDULE (BETULA ALBA L.)
Les feuilles de bouleau sont utilisées depuis l'Antiquité pour le traitement des rhumatismes, de la goutte et des maladies du système urinaire. Les tisanes sont préparées par décoction d'une ou deux cuillères à soupe de feuilles séchées par tasse d'eau, en ajoutant une pincée de bicarbonate de soude. L'infusion a une odeur aromatique et un goût amer. Elles contiennent des saponines, des huiles essentielles, des tanins et des antiseptiques végétaux (phytosides)
Les feuilles de bouleau ont des propriétés diurétiques reconnues, utiles dans le traitement des affections rhumatismales et de la goutte (acide urique). Il produit une élimination rénale qui n'irrite pas les reins. (usage interne) Traitement des œdèmes d'origine cardio-rénale. (usage interne) Active la fonction rénale. (usage interne)
PROPERTIES:
Diurétique, anti-inflammatoire, fébrifuge, astringent
INDICATIONS:
Troubles urinaires, rhumatismes, œdèmes, fièvre, dyskinésies biliaires
PRECAUTIONS:
Non décrites
Non décrit.
Précautions
CONTRAINDICATIONS: Non décrit
Non décrit
(SOURCE : VADEMECUM PLANTAS MEDICINALES PLAMECA) (SOURCE : VADEMECUM PLANTAS MEDICINALES PLAMECA) L'infusion de feuilles de bouleau est un puissant diurétique capable de dissoudre les calculs rénaux et vésicaux, pour lesquels il est recommandé d'ajouter une pincée de bicarbonate de sodium à l'infusion. (SOURCE : VADEMECUM PLANTAS MEDICALES PLAMECA) Non décrit
Utilisations : Utilisation :
Les teasins sont préparés par décoction d'une ou deux cuillères à soupe de feuilles séchées par tasse d'eau, en ajoutant une pincée de bicarbonate de soude. L'infusion a une odeur aromatique et un goût amer. Elles contiennent des saponines, des huiles essentielles, des tanins et des antiseptiques végétaux (phytosides)
Conservation
Conserver dans un endroit frais et sec, à l'abri des odeurs fortes et des sources de contamination Stockage
Stockage Conserver dans un endroit frais et sec, à l'abri des odeurs fortes et des sources de contamination. DECLARATION DES ALLERGES DECLARATION DES ALLERGES
Selon la fiche technique du ou des fournisseurs :
Il ne contient AUCUN GLUTEN EN TANT QU'INGRÉDIENT, Mais AUCUNE GARANTIE NE PEUT ÊTRE DONNÉE SUR L'ABSENCE DE TRACE.
ALLERGÈNES:
Ne contient aucun allergène comme ingrédients
En raison d'une contamination croisée, peut contenir Célériaque, noix, moutarde et sésame
Des processus de nettoyage et d'assainissement sont effectués tant dans nos installations que dans celles de nos fournisseurs après chaque production pour éviter toute contamination croisée, ainsi que des systèmes d'autocontrôle et de vérification pour confirmer l'absence de traces. Cependant, nous ne pouvons pas affirmer que les produits sont exempts d'allergènes présents dans la plante en raison d'une contamination accidentelle
DIRECTIVE COMMUNAUTAIRE 2006/142/CE RELATIVE AUX INGRÉDIENTS ET À L'ÉTIQUETAGE DES ALLERGÈNES Selon la directive 2003/89/CE, voici la liste des ingrédients allergènes qui doivent être mentionnés sur l'étiquetage à des fins de protection des consommateurs, car la présence de ces substances peut provoquer des allergies. DECLARATION DE NON-MODIFICATION GÉNÉTIQUE LÉGISLATION APPLICABLE
APTITUDE POUR LES GROUPES ETHNIQUES ET AUTRES:
HALAL convient : OUI, certificat officiel non disponible
Approuvé par les diététiciens : OUI
convient aux végétariens : Oui
Plaisant pour les végétariens : Oui
SUIT POUR LES CELIACS : NON
